Actualidad
El futuro de la inmunoterapia, a prueba en un chip
Imagina un órgano humano contenido en un espacio tan pequeño como una moneda de un euro. Imagina ahora que este órgano es invadido por células tumorales y que podemos analizar en tiempo real la respuesta del tumor a diversos tratamientos. Este tipo de sistemas es ya una realidad gracias a los chips microfluídicos. El investigador José María Ayuso Domínguez lo explica desde su laboratorio en la Universidad de Wisconsin-Madison (EEUU).
José María Ayuso Domínguez (Chema, para sus compañeros en España) se formó como bioquímico en la Universidad Autónoma de Madrid. Tras obtener su doctorado en el grupo de microentorno tisular de la Universidad de Zaragoza, emigró a Estados Unidos para participar en el desarrollo de una nueva tecnología que recrea órganos en el interior de estos chips / Sergio Camero
La temida palabra cáncer engloba a un grupo de más de 100 enfermedades distintas, muchas de ellas aún con mal pronóstico. La medicina moderna ha recurrido a las biopsias (muestras sólidas extraídas quirúrgicamente del paciente) para elegir un tratamiento acorde a cada caso. Ahora, la llegada de los chips al área de la oncología ha supuesto una revolución. Estos dispositivos analizan la sangre en busca de marcadores tumorales que circulan por todo el cuerpo. El uso de fluidos como una biopsia líquida, en lugar de la biopsia sólida convencional de un tumor, tiene muchas ventajas. Es un método menos invasivo, reduce la incomodidad del paciente y puede proporcionar información sobre tumores de difícil acceso.
“Las probabilidades de acertar en el tratamiento de un cáncer aumentan usando los modelos de tumor en chip”
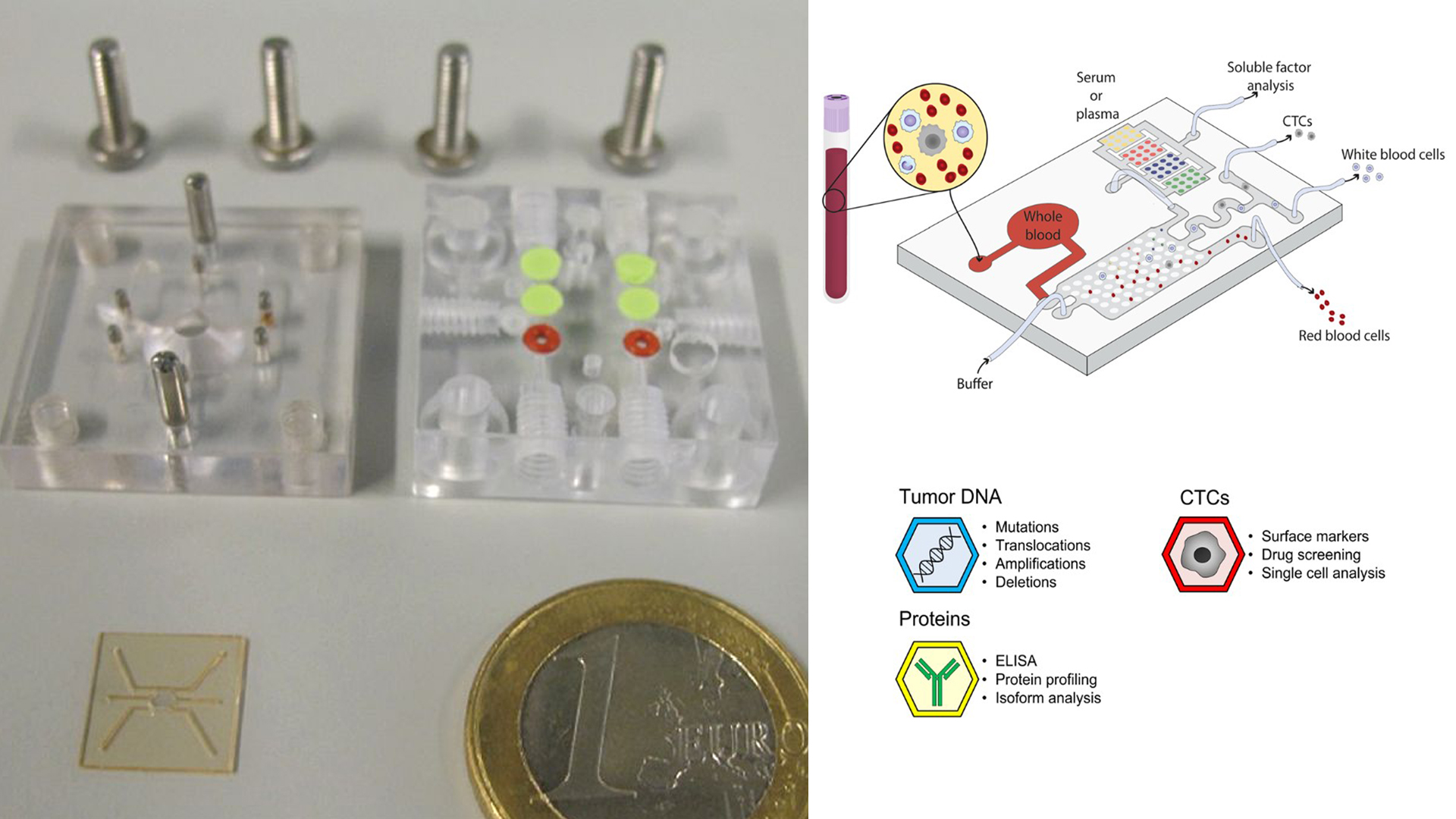
Modelos microfluídicos en un chip / José M. Ayuso et al. (2022)
Modelos de tumor en chip: nuevos laboratorios a escala microscópica
Según explica el doctor Ayuso, “en los chips microfluídicos podemos generar sistemas con condiciones geométricas, físicas y químicas similares a las que se encuentran in vivo en los órganos humanos. Estos modelos tridimensionales de tumor en chip introducen redes de vasos sanguíneos, células inmunes y recrean el tejido humano con mayor fidelidad. Las probabilidades de acertar en el diagnóstico y tratamiento de un cáncer suben con respecto a las técnicas clásicas que se han utilizado en medicina durante los últimos años”.
Asegura que este tipo de modelos supone un avance gigantesco a nivel experimental: “Hasta la llegada de los chips, en los laboratorios biológicos hacían ensayos con células sobre placas Petri y trataban de estudiar así los órganos, pero en realidad esto era una reducción demasiado simplista. Si te limitas a trabajar con un único tipo celular en una superficie plana, pierdes muchas propiedades que son fundamentales para entender cómo funciona el órgano”.
Lo explica de una manera muy gráfica con un ejemplo: “Del mismo modo que un pulmón para funcionar debe ser una cavidad tridimensional que se hincha, absorbe el aire y transmite el oxígeno a los tejidos, es imposible ver algo parecido cultivando células de pulmón en una placa con sólo dos dimensiones”. La llegada de los chips ha conseguido reproducir la estructura del pulmón y otros órganos tan complejos como hígado y riñones, permitiendo estudiar cómo se extiende un tumor en su interior.
Los tumores emplean una gran variedad de estrategias para escapar de las defensas del organismo. Gracias a los laboratorios en chip se puede estudiar en cada momento qué está ocurriendo en el microentorno de un tumor con todo lujo de detalles, lo que podría acelerar el desarrollo de nuevas terapias. Una de las más prometedoras es la inmunoterapia.
Entrenando al sistema inmune para vencer al cáncer
La inmunoterapia se basa en reforzar la respuesta inmune del propio paciente para eliminar tumores. Desde el laboratorio de modelos patológicos de la Universidad de Wisconsin-Madison, ensayan nuevas terapias inmunológicas contra el cáncer en el interior de estos chips: “Estos sistemas tienen indudables ventajas dado que recrean estructuras fisiológicas y tumorales de una manera más realista que las técnicas tradicionales de cultivo celular en placa. Además, nos permiten trabajar con cantidades mínimas de muestra” sostiene el doctor Ayuso.
Su reciente artículo publicado en Science Advances ha sido seleccionado como uno de los más interesantes en este campo por la revista y ha tenido gran repercusión en la comunidad científica. Trata un fenómeno denominado extenuación inmunológica: la incapacidad del sistema inmune para luchar contra un tumor a largo plazo.
En sus propias palabras: “El sistema inmune ha evolucionado para lidiar con amenazas o infecciones que se resuelven en el periodo de unos días. Del mismo modo que nos ocurre a las personas, si las células inmunes tienen que defenderse contra una amenaza durante meses o incluso años, al final se cansan. Esta pérdida de eficacia contra un tumor se conoce como extenuación inmunológica y la podemos analizar en tiempo real dentro de nuestros modelos de tumor en un chip”.
“Estamos desarrollando una nueva generación de células inmunes menos sensibles al cansancio inmunológico”
Estos chips microfluídicos simulan un escenario parecido al de un tumor, donde escasean el oxígeno y los nutrientes. En uno de sus modelos de tumor han comprobado que este estrés generado anula a las llamadas células NK (del inglés Natural Killer), un tipo de célula inmune que elimina células cancerosas. Observaron que, en un periodo muy corto de tan sólo 7 días, la capacidad de estas células para atacar al tumor se reducía. Pero para su sorpresa, la extenuación resultó ser parcialmente reversible. Al tratar las células NK con una mezcla de nutrientes y fármacos experimentales, consiguieron aliviar en parte la extenuación y recuperar cierta actividad antitumoral.
Animado por los resultados, el grupo de investigación quiere llegar aún más lejos y seguir perfeccionando la técnica en el futuro: “Nuestro objetivo es conseguir una nueva generación de células inmunes entrenadas para reconocer y eliminar tumores de manera más eficaz. Mediante ingeniería genética modificamos las células para hacerlas menos sensibles al cansancio inmunológico que genera el tumor”.
_____________________
Sergio Camero Gigante es licenciado en bioquímica y doctor en biofísica por la Universidad Autónoma de Madrid. Ha trabajado como personal investigador de apoyo en el Laboratorio de Espectroscopia de RMN "Manuel Rico" del Consejo Superior de Investigaciones Científicas y actualmente cursa el Título de Experto en Comunicación Pública y Divulgación de la Ciencia en la UAM.
_____________________
Referencia bibliográfica:
Ayuso, J.M., Virumbrales-Muñoz, M., Lang, J.M., Beebe, D.J. 2022. A role for microfluidic systems in precision medicine. Nature Communications 13, 3086. doi: 10.1038/s41467-022-30384-7
Más cultura científica en UAM Gazette.